백신 임상시험 자료에 대한 안전성·효과성 검토
오미크론 변이 대응 위해 개발… 추가접종 사용
오미크론 변이 대응 위해 개발… 추가접종 사용
 이미지 확대보기
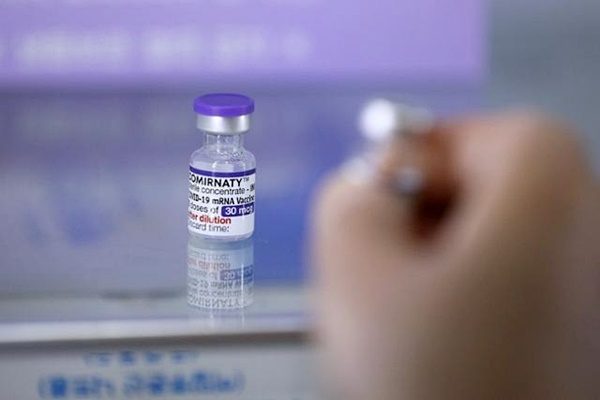
이미지 확대보기'코미나티2주0.1㎎/㎖'는 한국화이자제약이 오미크론 변이에 대응하도록 개발한 백신이다. 초기 코로나19 바이러스(우한주)와 변이 바이러스(오미크론주·BA.1)의 항원을 각각 발현하는 메신저리보핵산(mRNA)을 기반으로 한다. 기존 백신을 기초 접종한 후 추가접종(부스터샷)하는 데 사용된다.
식약처는 제출된 임상 자료를 신속하고 면밀하게 검토할 예정이다. 아울러 비임상·품질 등 자료를 추가해 품목 허가를 신청할 경우 감염내과 전문의를 포함한 백신 전문가 등에 안전성·효과성을 자문하겠다고 밝혔다.
사전검토 결과 백신의 안전성과 효과성이 증명되면 허가신청 단계를 밟게 된다. 이 경우, 무난한 통과가 예상된다. 방역당국에서 이달 말 오미크론 개량 백신을 활용한 하반기 접종 전략을 발표할 예정인 만큼 부스터샷으로 바로 투입될 가능성이 높다.
한편, '코미나티2주0.1㎎/㎖'는 유럽 등에서도 사전검토가 진행 중이다.
소미연 글로벌이코노믹 기자 pink2542@g-enews.com



























